|
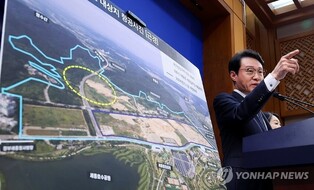
| (사진=연합뉴스) |
[알파경제=박남숙 기자] 알테오젠(0196170)이 한국 바이오 역사상 최초로 국내 플랫폼이 전세계 매출 1위 블록버스터 의약품에 장착되어 FDA로부터 승인을 획득했다.
이는 당초 예정된 일정보다 3일 빠른 결정으로 출시도 10월 1일 아닌 9월 말로 잡혔다. 유럽도 내년 상반기에서 반기 빨라진 4분기 승인 예정으로 전세계 승인도 마무리 수순이다.
신한투자증권에 따르면, 머크와 알테오젠 공동개발 제품명은 ‘키트루다 Qlex’로 출시했다.
BMS/할로자임 옵디보SC 5분, 로슈/할로자임 티쎈트릭 7분 대비 가장 빠른 1~2분 투여한다.
티쎈트릭SC는 7분 걸림에도 영국 출시 9개월만에 32% SC로 전환에 성공했다. 머크의 2년 내 30~40% 시장 SC 전환은 보수적 목표란 판단이다.
엄민용 신한투자증권 연구원은 "IV 3주 제형과 6주 제형 동시 승인된 것 또한 서프라이즈"라며 "투여 6주 간격은 SC 제형 중 유일하다"고 평가했다.
BMS 옵디보는 2~4주, 로슈 티쎈트릭은 3주 간격만 SC 승인, 19일 유럽 CHMP 승인 권고를 발표하며 유럽도 4분기 승인이 유력하다.
키트루다IV가 가진 모든 적응증에 대해 키트루다SC를 승인한 것은 서프라이즈로 빠른 SC 교체위해 중요했던 2가지 용량 및 모든 적응증 승인을 완료했다.
엄민용 연구원은 "지난 2021년 10월 임상 개시 후 부터 승인까지 만 4년이라는 유례없는 속도로 머크는 사활을 걸고 진행 중"이라며 "이번 3분기 중 FDA 승인에 따른 수백억원 단계별 마일스톤 인식 공시도 예상된다"고 밝혔다.
첫 판매 마일스톤은 알테오젠 4분기 실적에 바로 인식될 것으로 보인다.
엄 연구원은 "코스피 이전을 위한 모든 조건이 마련됐다"며 "빅파마와 연내 1~2건 기술이전 목표를 유지 중으로 이번 FDA 승인 여부가 계약 상대의 마지막 의사 결정 요소여서 지금까지 발표가 없었다고 본다면 곧 L/O 공시도 기대 가능하다"고 전망했다.
알파경제 박남숙 기자(parkns@alphabiz.co.kr)